【美国不加入与世卫有关的疫苗开发】于2020年09月02日,据鸭寮街了解到,现在全球对新冠疫苗都非常期待,而很多国家也加入了合作研发疫苗的联盟,期望能够尽快战胜疫情,而一向霸道的美国却称不会加入跟世卫有关的疫苗研发,因为不想受到世卫和我国的约束,这番言论出来之后也引起了很多人的不满,大家都认为美国太过自负了,除此以外,美国还考虑紧急授权新冠疫苗,但这样的话,新冠疫苗的功效和安全性就不能得到保障。接下来,大家可以和鸭寮街小编一起详细了解一下哦~
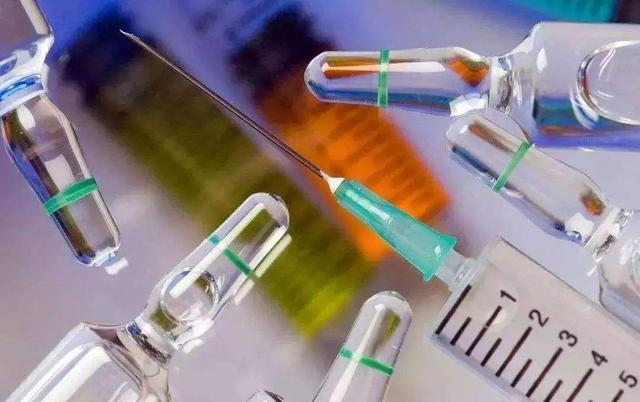
美国不加入与世卫有关的疫苗开发
据美国《华盛顿邮报》9月1日报道称,美国不会加入一个全球合作研发疫苗的联盟,部分原因是白宫不想和世卫组织合作。美国白宫副新闻秘书贾德·迪雷说:“美国将继续和我们的国际伙伴合作抗疫,但我们不会被一些受到世卫组织和中国影响的多边组织所约束。”
报道称,目前全球有超过170个国家和地区正在谈判加入新冠疫苗全球渠道计划(COVAX),该计划得到了世卫组织、其他疫苗开发组织以及美国传统盟友的支持,包括日本德国和欧盟,但美国则不会加入。报道中,乔治城大学全球卫生法学教授Lawrence Gostin说:“美国采取了一种单独行动的策略,这是一场巨大的赌博。”
美国考虑快速批准新冠疫苗 世卫组织官员:动作太快有风险
海外网9月1日电美国宣布考虑快速批准疫苗后,世界卫生组织当地时间8月31日表示,新冠肺炎疫苗的紧急授权需要全方面权衡利弊。
据加拿大《环球新闻》报道,世卫组织首席科学家苏米亚·斯瓦米纳坦(Soumya Swaminathan)在新闻发布会上表示,虽然每个国家都有权在没有完成全面试验的情况下批准,“但这不是一个可以轻易做出的决定”。苏米亚·斯瓦米纳坦(Soumya Swaminathan)表示,世卫组织推荐的首选方法是拥有一套完整的数据,可用于疫苗的预审。世卫组织随后将根据个案情况考察每种药物的功效和安全性。
世卫组织紧急情况项目负责人迈克尔·J·瑞安 (Michael J. Ryan)表示,世卫组织已经使用实验性药物在非洲对抗埃博拉,这一措施被证明是成功的。但他强调,在没有进行全面试验的情况下采取快速通道的方法,需要进行密集的监测和安全后续工作,如果出现问题,应立即停止,“如果你动作太快,给数百万人接种疫苗,可能会漏掉某些不良反应。”
美国食品和药物管理局局长斯蒂芬·哈恩8月30日透露,为尽快推出新冠疫苗,他愿意跳过部分常规的审批环节。加拿大总理特鲁多也表示,加拿大希望走在新冠肺炎疫苗研发的领先地位,并已在当地时间8月31日与诺瓦克斯和强生签署了实验新冠肺炎疫苗的协议。特鲁多表示,加拿大有大约3800万人口,到目前为止签署的四项疫苗协议为加拿大提供了至少8800万剂疫苗。
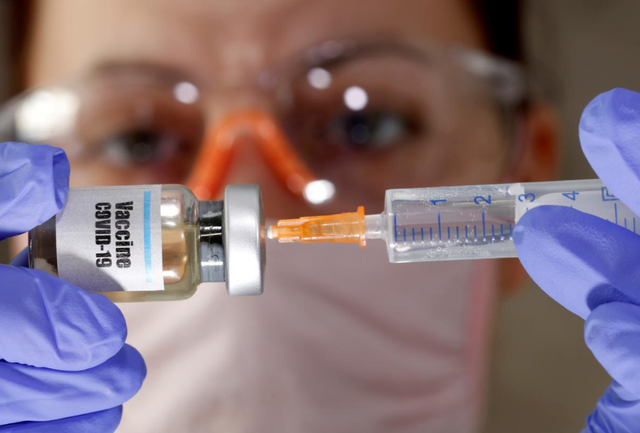
世卫组织:6种疫苗进入三期临床试验 3种来自中国
8月7日,据媒体报道,世卫组织表示,目前全球6种疫苗已进入三期临床试验,其中3种来自中国。
当地时间8月6日,世卫组织召开新冠肺炎例行发布会,世卫组织卫生紧急项目负责人迈克尔·瑞安称,目前全球约有165种疫苗处于试验阶段,26种进入临床试验阶段,6种已处于三期临床试验阶段,其中3中来自中国。
瑞安表示,疫苗进入三期临床试验并不意味着研发成功,三期只意味着疫苗将投放到人群中,用在健康的民众身上,以观察疫苗是否能够保护他们免受天然感染。
瑞安指出,到目前为止,所有的疫苗研究都围绕着安全性、免疫原性展开,并要确保疫苗在小部分人群中激发免疫反应,并且不会产生妨碍疫苗进入实验阶段的不良反应,从这个意义上说,疫苗要通过一关又一关考验,我们希望会有更多的疫苗研究能进入这些临床试验阶段。
药物临床试验分为I、II、III、IV期。III期临床试验是治疗作用确证阶段。其目的是进一步验证药物对目标适应症患者的治疗作用和安全性,评价利益与风险关系,最终为药物注册申请的审查提供充分的依据。
而IV期临床试验为新药上市后应用研究阶段。其目的是考察在广泛使用条件下的药物的疗效和不良反应,评价在普通或者特殊人群中使用的利益与风险关系以及改进给药剂量等。
据悉,我国目前的3种进入三期临床试验的新冠疫苗分别是:国药武汉生物制品研究院的灭活疫苗、科兴生物开发的灭活疫苗以及陈薇院士团队开发腺病毒载体疫苗。
外媒:要当心了!新冠疫苗可能对这类人群疗效不佳
据阿根廷布宜诺斯艾利斯经济新闻网8月29日报道,尽管全世界都对新冠病毒疫苗翘首以待,但来自不同国家的专家对这种药物或将无法满足风险最高的人群之一肥胖人群的需求而深表担忧。
自新冠病毒开始大流行以来,一些研究表明,体重指数高的人感染病毒和死亡的风险较高。
报道称,现在,随着使用不同候选疫苗的试验不断推进,专家担心这些潜在疫苗无法保护这一风险人群,因为科学证据表明以前的一些疫苗(例如流感、乙型肝炎、破伤风和狂犬病)的药效在肥胖人群中会降低。
美国生物医疗上市公司研制的新冠疫苗最先进的试验中心之一马里兰大学医学院的首席研究员马修·B·劳伦斯博士在最近的一次采访中承认:“我们已经知道的是,其他一些疫苗在肥胖人群中的测试效果不佳。”
报道称,“尽管我们正在开发新冠疫苗,但我们认识到它可能不适用于所有人群,包括肥胖人群。因此,这是一个很大的问题,”他补充说。
尽管科学家仍在研究肥胖症患者可能无法对疫苗接种产生预期反应的确切的生物学机制,但专家指出,慢性炎症似乎会干扰疫苗的免疫反应,因此,肥胖者即使在免疫后也更容易遭受疾病的侵袭。
为了买得起疫苗,各国各显神通
还在疫苗研发上绞尽脑汁的科学家们或许想不到,对很多人来说,难倒他们的其实是疫苗价格。对于一些人口大国来说,要给本国超过60%(编注:达到“群体免疫”的人口百分比)的人接种疫苗,花费不菲。
据哈萨克斯坦光明网8月13日报道,俄罗斯R制药集团公司(R-Pharm)董事长列比克在接受采访时表示,首批上市的新冠肺炎疫苗价格较高,用于出口的疫苗平均价格约为2剂10美元。俄罗斯计划于9月初开始大规模生产疫苗,10月前数十万支疫苗将首批上市,年底前开始在其他国家销售。
而10美元两剂的价格也已经要比其他国家一些候选疫苗便宜很多。
据《金融时报》报道,自从生物技术公司莫德纳(Moderna)与美国国家过敏症和传染病研究所合作研发的疫苗初步显示出有效性并成为美国首支进入临床试验的疫苗以来,莫德纳的股价今年已飙升近325%。目前,美国政府已为该疫苗的研发投入近25亿美元。而据了解莫德纳与潜在买家谈判情况的人士透露,该公司将其疫苗的价格定为每疗程约50至60美元,高于其他疫苗生产商与美国政府达成的疫苗订购价。一些熟悉莫德纳疫苗销售计划的人士表示,这一定价将适用于美国以及其他高收入国家——也就是说,该公司打算优先向这些国家供应疫苗。
报道称,影响公司为其药品和疫苗定价的因素有很多,包括提交监管申请的时机、医疗需求、疗效和竞争情况。一位了解莫德纳计划的人士表示,该公司报价较高是因为考虑到订单规模和交货时间。
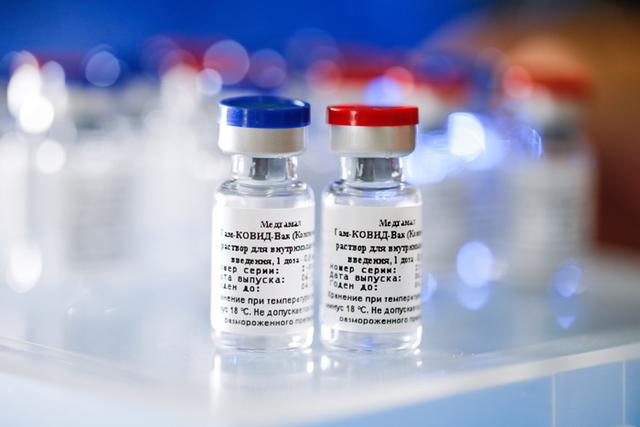
我国疫苗研发到了哪一步?
记者从国务院联防联控机制了解到,我国4款新冠病毒疫苗已开启国际Ⅲ期临床试验,部分试验将在9月初完成首轮接种。
Ⅲ期临床试验是确定疫苗能否获批上市的关键研究,将真正验证疫苗的安全性和有效性,需要数千至上万人的样本量。据悉,已启动的新冠病毒疫苗Ⅲ期临床试验预计最快可在11月前获得初步数据。
中国生物技术股份有限公司董事长杨晓明介绍,该企业研发的两款新冠病毒灭活疫苗目前已在中东、南美多个国家获批开展Ⅲ期临床试验,试验入组总人数超过3万人。
北京科兴中维生物技术有限公司董事长尹卫东介绍,该企业研发的一款新冠病毒灭活疫苗正在南美、东南亚几个国家稳步推进Ⅲ期临床试验。
此外,军事科学院军事医学研究院陈薇团队研发的腺病毒载体重组新冠病毒疫苗也正在有序推进国际Ⅲ期临床试验。
由于新冠肺炎疫情目前在我国得到有效控制,国内已不具备大规模临床试验的客观条件,因此上述Ⅲ期临床试验均在海外进行。
打完疫苗能管用多久?
根据已经结束的Ⅰ期、Ⅱ期临床试验结果,多款新冠病毒疫苗体现出良好的安全性,也显示出抗体有效性。
杨晓明介绍,中国生物的两款疫苗于4月陆续获批启动Ⅰ期、Ⅱ期临床试验,试验结果显示,接种两剂疫苗后,中和抗体阳转率均达100%。
这些抗体能持续多久?答案仍有待Ⅲ期临床试验的验证。
与此同时,一批科研人员正在汇总国内疫情暴发期间感染新冠病毒并康复的病例数据,分析其体内抗体的持续时长,试图从机理上解答“会否二次感染新冠病毒”这一问题。
根据近日国家药监局药审中心发布的《新型冠状病毒预防用疫苗临床评价指导原则(试行)》文件,对于新冠病毒疫苗的有效性专门提出:疫苗最好能提供1年及以上的保护,至少提供6个月的保护。
以上是【美国不加入与世卫有关的疫苗开发】的详细全文内容,对于美国不加入与世卫有关的疫苗开发你有什么看法呢?
郑重声明:版权归原作者所有,本文仅为生活热点内容更加丰富,非鸭寮街观点。如信息标记有误,欢迎联系我们修改或删除,多谢合作。







